|
|
▎药明康德/报道
在ESMO 2019大会上,最受关注的研发进展之一是PARP抑制剂在卵巢癌患者中的表现。PARP抑制剂是通过抑制PARP介导的DNA损伤修复反应(DDR),杀伤癌细胞的靶向疗法。利用“合成致死”原理,它们能够在杀伤癌细胞的同时,不对健康细胞产生影响。目前,已经有4款PARP抑制剂获得FDA批准上市。最初它们被认为只对携带BRCA基因突变的癌症有效,然而,阿斯利康(AstraZeneca)公司和葛兰素史克(GSK)公司最近分别宣布,Lynparza和Zejula在临床试验中在不携带BRCA基因突变的卵巢癌患者中表现出疗效。今日,两家公司在ESMO上公布了试验的详细数据。

Zejula
Zejula是GSK收购TESARO获得的PARP抑制剂。扩展Zejula的适用患者群是GSK的研发重心之一。在名为PRIMA的临床试验中,接受铂基化疗获得缓解的晚期卵巢癌患者接受了Zejula或安慰剂的维持治疗。

试验结果表明,无论患者的生物标志物状况如何,Zejula将患者疾病进展或死亡风险降低38%(HR=0.62, 95% CI, 0.50-0.75, p<0.001),Zejula组PFS为13.8个月,对照组为8.2个月。其中:
携带BRCA基因突变患者的风险降低60%(HR=0.40, 95% CI,0.27-0.62,p<0.001)。
携带野生型BRCA基因但是具有同源重组缺陷(HR-deficient)的患者的风险降低50%(HR=0.50,95% CI,0.30-0.83,p=0.006)。
同源重组正常的患者风险降低32%(HR=0.68,95% CI,0.49-0.94,p=0.020)。
对患者总生存期的分析尚未成熟,但是接受Zejula治疗的患者与对照组相比,总生存率显示出提高的趋势。
GSK首席科学官兼研发总裁Hal Barron博士表示:“PRIMA临床试验是一个具有里程碑意义的研究。我们相信这些数据有潜力从根本上改变治疗卵巢癌患者的方式!”
Lynparza
阿斯利康的Lynparza(olaparib)是第一款获得FDA批准的PARP抑制剂。在名为PAOLA-1的随机双盲临床试验中,接受铂基化疗并且进入完全或部分缓解的卵巢癌患者,接受了Lynparza+bevacizumab或bevacizumab的治疗。Bevacizumab是治疗这类患者的标准疗法。

试验结果表明,在意向治疗患者群中,Lynparza与bevacizumab构成的组合疗法,与活性对照组相比,为患者的无进展生存期(PFS)带来统计显著且具有临床意义的改善。接受Lynparza组合疗法的患者PFS达到22.1个月,显著高于对照组的16.6个月,将患者疾病进展或死亡风险降低41%(HR=0.59,p<0.0001)。
在携带BRCA基因突变的患者群中,Lynparza组合疗法将疾病进展或死亡风险降低69%(HR=0.31);
在具有同源重组缺陷的患者群中,Lynparza组合疗法将疾病进展或死亡风险降低67%(HR=0.33);
这两个患者亚群的中位PFS均为37.2个月。
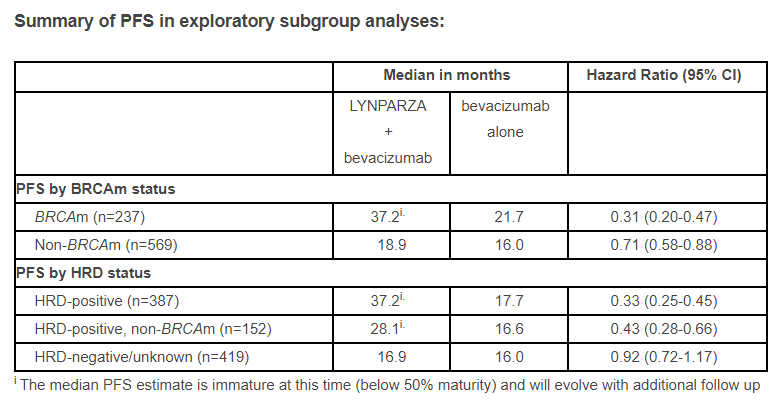
▲PAOLA-1临床试验不同患者亚群PFS分析结果(图片来源:参考资料[4])
阿斯利康肿瘤学研发执行副总裁José Baselga博士表示:“这一临床试验的设计旨在反映日常临床实践,将全球性标准疗法与Lynparza联用。我们将与监管部门合作,尽快将Lynparza带给相关患者。”
安进KRAS抑制剂治疗结直肠癌疾病控制率92%
在9月初的世界肺癌大会上,安进(Amgen)公司的KRAS G12C抑制剂AMG 510在治疗携带KRAS G12C突变的非小细胞肺癌患者中表现出50%的缓解率和100%的疾病控制率。今天,该公司公布了AMG 510治疗结直肠癌和阑尾癌患者的积极结果。
KRAS基因是人类癌症中最常见的致癌基因。KRAS G12C基因突变除了在13%的肺癌患者中出现以外,还在3%的结直肠癌和阑尾癌患者中出现。AMG 510是一款“first-in-class” KRAS G12C突变体共价抑制剂。它能够将KRAS永久锁定在与GDP结合的失活状态,从而抑制KRAS的活性。
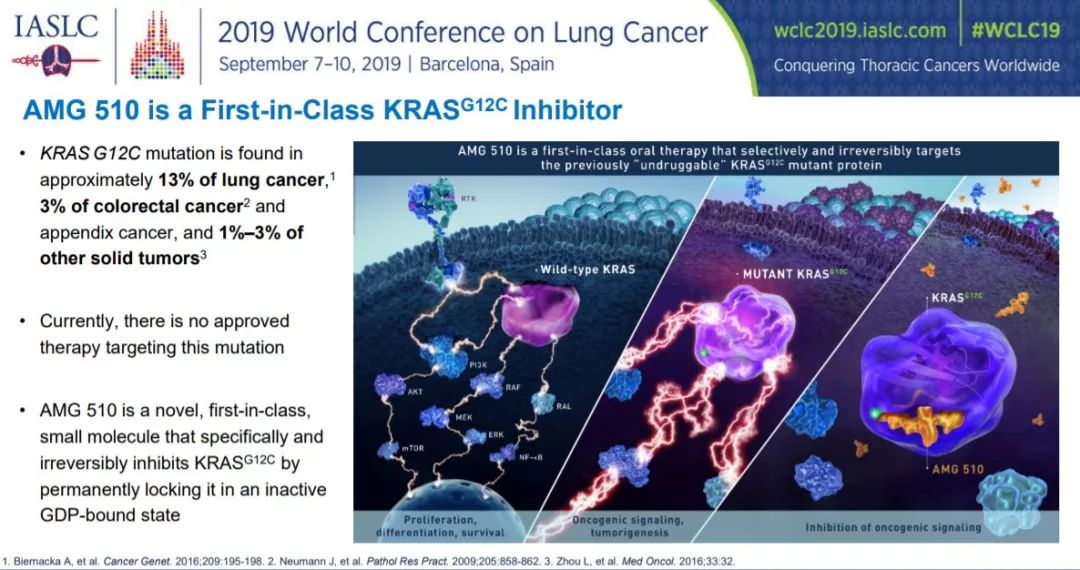
图片来源:安进公司官网
在ESMO上安进公布的数据包括55名能够评估疗效的患者,其中包括29名CRC患者。12名CRC患者接受了剂量为960 mg的AMG 510治疗。其中一名患者达到部分缓解,10名患者达到疾病稳定,疾病控制率为92%,目前仍然有10名患者在接受治疗。
在13名NSCLC接受960 mg AMG 510的NSCLC患者中,7名达到部分缓解,6名达到疾病稳定,疾病控制率为100%。在两名能够被评估的阑尾癌患者中一名达到部分缓解,另一名疾病稳定。
“虽然KRAS G12C在过去四十年来一直是一个难以攻克的难关,但是现在我们报告非小细胞肺癌、结直肠癌和阑尾癌患者都可以获得缓解,”安进公司研发执行副总裁David M. Reese博士说:“这些结果非常令人鼓舞,尤其是因为这些患者已经平均接受过4种前期疗法,有些患者接受过高达10种疗法。我们正在启动组合疗法研究,进一步探索AMG 510治疗肺癌和结直肠癌的潜力。”
“晚期结直肠癌患者的预后非常不良,”这一临床研究的研究员,加州希望之城胃肠道癌症项目联合主任Marwan G. Fakih博士说:“这些接受过多种治疗的结直肠癌患者通常中位无进展生存期只有2个多月,看到他们在3个月之后仍然在接受治疗非常令人鼓舞。”
参考资料:[1] Amgen Announces New Clinical Data Evaluating Novel Investigational KRAS(G12C) Inhibitor In Patients With Solid Tumors At ESMO 2019. Retrieved September 27, 2019, from https://www.amgen.com/media/news-releases/2019/09/amgen-announces-new-clinical-data-evaluating-novel-investigational-krasg12c-inhibitor-in-patients-with-solid-tumors-at-esmo-2019/[2] Phase 3 PRIMA trial of Zejula? (niraparib) is the first study to show a PARP inhibitor significantly improves PFS, regardless of biomarker status, when given as monotherapy in women with first-line platinum responsive advanced ovarian cancer. Retrieved September 28, 2019, from https://www.gsk.com/en-gb/media/press-releases/phase-3-prima-trial-of-zejula-niraparib-is-the-first-study-to-show-a-parp-inhibitor-significantly-improves-pfs-regardless-of-biomarker-status/[3] PRIMA vs PAOLA: GSK and Merck/AstraZeneca square off in a high-profile PARP showdown at ESMO. Retrieved September 28, 2019, from https://endpts.com/prima-vs-paola-gsk-and-merck-astrazeneca-square-off-in-a-high-profile-parp-showdown-at-esmo/[4] LYNPARZA? (olaparib) Phase 3 PAOLA-1 Trial Significantly Increased Progression-Free Survival as First-Line Maintenance Treatment with Bevacizumab for Newly-Diagnosed Advanced Ovarian Cancer. Retrieved September 28, 2019, from https://www.businesswire.com/news/home/20190928005021/en/LYNPARZA%C2%AE-olaparib-Phase-3-PAOLA-1-Trial-Significantly
版权说明:本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「药明康德」微信公众号回复“转载”,获取转载须知。

|
|